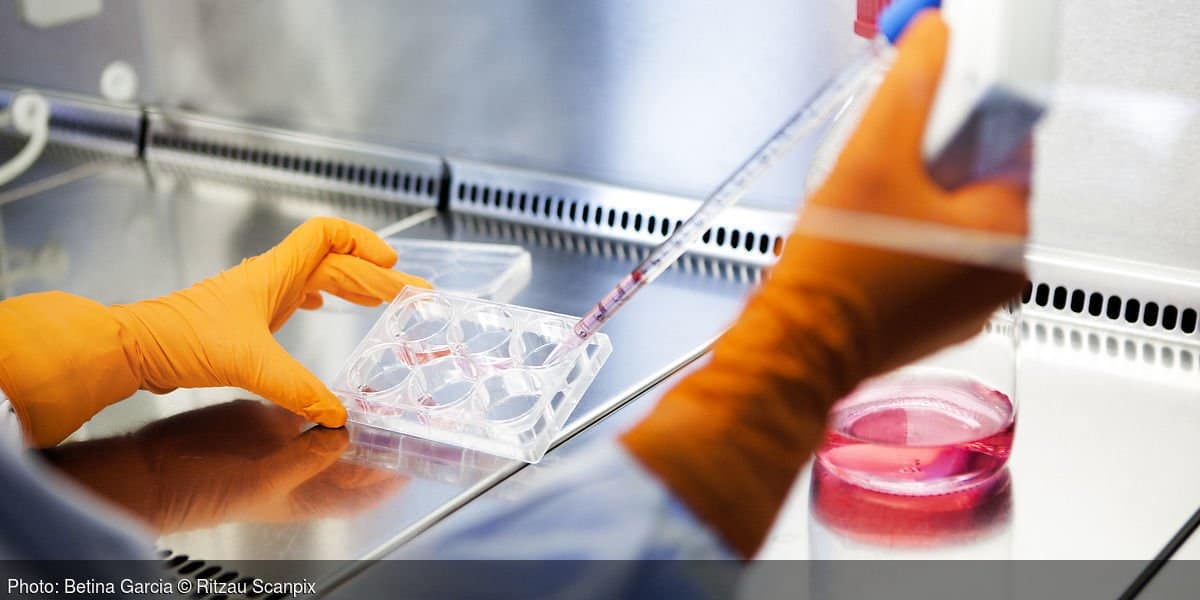
Fra Bavarian:
KØBENHAVN, Danmark, 23. august 2021 – Bavarian Nordic A/S (OMX: BAVA) meddelte i dag, at selskabet har indgået en aftale med det danske sundhedsministerium (”Sundhedsministeriet”) om finansiering af videreudviklingen af selskabets COVID-19 vaccinekandidat, ABNCoV2.
Aftalen har en værdi af op til DKK 800 mio. og sigter mod at understøtte udviklingen frem til godkendelse af ABNCoV2 som en boostervaccine, der kan bidrage til at styrke forsyningssikkerheden af COVID-19 vacciner til at imødekomme behovet for revaccination af befolkningen.
I henhold til aftalen modtager Bavarian Nordic en forudbetaling på DKK 80 mio. samt betalinger på op til DKK 720 mio., der er betinget af opnåelsen af en række foruddefinerede milepæle, herunder blandt andet afslutningen af det igangværende fase 2-forsøg, fase 3 udviklingsmilepæle samt milepæle knyttet til opskalering af den kommercielle produktion af vaccinen.
Aftalen er betinget af den endelige godkendelse af Folketingets Finansudvalg.
Alle betalinger er potentielt tilbagebetalingspligtige, dog kun ved succesfuld opnåelse af markedsføringstilladelse fra Europa-Kommissionen. Tilbagebetaling kan ske via levering af vacciner samt royaltybetalinger fra salget af vacciner til andre kunder. Royaltybetalinger vil kun blive udløst ved opnåelse af en vis salgsvolumen. Sundhedsministeriet vil desuden kunne modtage en yderligere, begrænset royaltybetaling, såfremt salget af vaccinen når et vist niveau over den volumen, der udløser den almindelige royaltybetaling.
Paul Chaplin, administrerende direktør i Bavarian Nordic, udtaler: “Vi er særdeles tilfredse med opnåelsen af denne aftale med Sundhedsministeriet, som muliggør videreførelse af udviklingen af vaccinen frem mod godkendelse. Aftalen er en stor anerkendelse af ABNCoV2’s potentiale som en universel boostervaccine, og vi er stolte over at videreføre bestræbelserne af den danske forskning, som har vist lovende resultater i de hidtidige prækliniske og kliniske forsøg. Vores igangværende fase 2-forsøg vil bidrage med yderligere effektdata på anvendelsen af vaccinen som en booster senere i 2021, hvilket sætter os i stand til at færdiggøre designet af fase 3 samt diskussionerne med de regulatoriske myndigheder inden forventet påbegyndelse af det afgørende forsøg i 2022.”
Aftalen forventes ikke at påvirke selskabets regnskabsmæssige forventninger for 2021.
Om ABNCoV2
ABNCoV2 tilhører en ny generation af COVID-19 vaccinekandidater, og er oprindeligt udviklet af AdaptVac på deres capsid virus like particle (cVLP)-teknologi. Bavarian Nordic har erhvervet de globale kommercielle rettigheder til vaccinen og har overtaget ansvaret for den videre udvikling frem mod godkendelse.
ABNCoV2 har vist sig at være yderst immunogen i relevante prækliniske modeller, hvor vaccinen har vist at kunne yde vedvarende og høj beskyttelse mod COVID-19 i et challenge-forsøg. Foreløbige resultater fra det første forsøg med i mennesker har bekræftet vaccinens evne til at fremkalde høje og brede antistofniveauer, der er bedre end dem, der er rapporteret for de godkendte vacciner. Samtidig viser resultaterne også, at vaccinen har en favorabel bivirkningsprofil. Desuden bekræfter resultaterne potentialet for ABNCoV2 til at fremkalde neutraliserende antistoffer mod SARS-CoV2 varianter, herunder Delta-varianten.