Med et indeks-fald over de seneste tre uger på 2,4% i det nordiske Healthcare indeks, ligger der fortsat en underliggende negativ stemning i sektoren.
Særligt negativ har stemningen været i den norske Healthcare sektor, hvor indekset er faldet med hele 16%. Faldene i Danmark og Finland har ligget på hhv. 2,3% og 2,6%, mens den svenske sektor performet bedst med et fald på blot 0,7%.
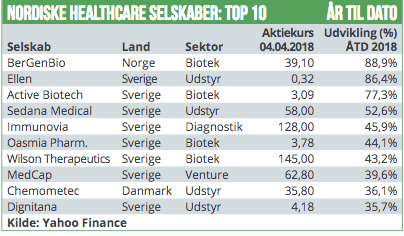
Blandt selskaberne finder vi Sedana Medical (+40%) og Immunovia (+27%) som højdespringerne. Sedana Medical er steget på baggrund et stærkt årsregnskab, der viser en pæn tocifret vækst i omsætningen og en stigende interesse i dets medical device AnaConDa. Immunovia har nydt godt af en børsopgradering til OMX Nasdaq, som har betydet større eksponering for aktien.
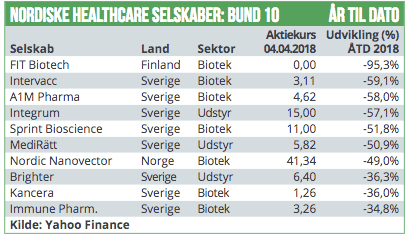
De største kursfald har ramt en række selskaber som foran kapitalrejsninger, herunder Kancera (-38%) og Annexin Pharmaceuticals (-28%). Desuden er det norske biotekselskab Nordic Nanovector faldet med 32% efter meddelelsen om et halvt års forsinkelse i dets førende cancer-udviklingsprogram.
Annexin Pharmaceuticals planlægger gennemfø-relsen af en emission med fortegningsret for eksisterende aktionærer med henblik på at rejse ca. 52 mio. SEK. samt potentielt yderligere 26 mio. SEK fra medfølgende tegningsoptioner (warrants). Emissionen er 100% garanteret af Annexins nuværende aktionærkreds. Såfremt warrants også udnyttes vil Annexin Pharmaceuticals havde sikret driften frem til udgangen af 2019. Emissionen ventes gennemført i maj måned og de nye aktier udstedes til kurs 4,40 SEK per aktie. Formålet med emissionen er at sikre kapital til den fortsat udvikling af selskabets
primære pipelineprojekt ANXV inden for hjerte/kar sygdomme. Annexin har specifikt valgt at fokusere udviklingen af ANXV inden for sygdommen Central Retinal Vein Occlusion (CRVO), som dækker over en blokering i hovedvenen i nethinden, der i værste fald kan føre til blindhed. Annexin Pharmaceuticals forventer at starte fase I forsøg i raske frivillige i lø-bet af sommeren 2018 samt at starte fase II studie i CRVO-patienter inden udgangen af 2019. Annexin Pharmaceuticals aktiekurs er faldet med 28% de seneste tre uger på udsigten til aktieudvanding og handles nu i -31% for hele 2018.
AstraZeneca meddeler at de europæiske sundhedsmyndigheder (EMA) har accepteret at påbegynde review af selskabets indsendte registreringsansøgning for PARP-hæmmeren Lynparza, som en behandling af BRCA-muteret og HER-2 negative metastatisk bryst-cancer hvor patienterne tidligere har modtaget kemoterapeutisk behandling. Fase III forsøg (OlympiAD studiet) viste, at Lynparza forlængede den progressionsfri-overlevelse (PFS) med 42% i forhold til standard kemoterapi. Dette modsvarede en median PFS på 7,0 måneder for Lynparza vs. 4,2 måneder for kemoterapi-armen. I januar 2018 er Lynparza allerede blevet godkendt af FDA i USA ligeledes i metastatisk brystkræft. Desuden er Lynparza godkendt i 60 lande som behandling af ovarie-cancer. AstraZeneca har også fået accepteret review af en FDA-ansøgning for CD-22 immun-toxin antistoffet Moxetumomab pasudotox i USA. Ansøgningen dækker Hairy Cell Leukaemia (HCL) og baseres på positive data fra et fase III studie i patienter, som havde modtaget mindst to forudgående typer behandling.
Forsøget ramte primary endpoint og viste således en acceptabel varig responsrate (konkrete forsøgsresultater fortsat ikke fremlagt). FDA har tildelt Moxetumomab pasudotox såkaldt Priority Review Status, hvilket betyder, at der ventes en endelig beslutning om godkendelse allerede i Q3 2018. Endelig har AstraZeneca modtaget markedsgodkendelse i Europa for Lokelma (tidligere kendt som ZS-9, sodium zirconium cyclosilicate) som en behandling af voksne patienter med Hyperkaliæmi, dvs. forhøjede niveauer af kalium i blodet. Der ventes desuden en FDA-beslutning om markedsgodkendelse af Lokelma i USA i løbet af Q2 2018. I tre stk. fase III studier har Lokelma påvist normalisering af kalium-niveauet inden for 2,2 timer i gennemsnit og 98% opnåede normaliseret kalium inden for 48 timer. AstraZeneca aktien har reageret kraftigt positivt på nyhedsstrømmen og er steget med 6% de seneste uger. Dermed er aktien nu i et plus på 3% siden nytår.
BioInvent har afsluttet en rettet emission, der har rejst et samlet bruttoprovenu på 85 mio. SEK. I alt er 45,7 millioner nye aktier til en tegningskurs på 1,85 SEK per aktie udstedt. Dermed stiger det samlede antal udestående aktier med 13% til 350,4 millioner aktier. BioInvents to største aktionærer van Herk Investments B.V. og Omega Fund IV deltog i emissionen og desuden har man formået at tiltrække nye lifescience specialiserede institutionelle investorer herunder Rhenman Healthcare Equity L/S. Provenuet fra emissionen vil blive anvendt på videreudvikling af den førende antistofbaserede udviklingskandidat BI-1206 inden for hematologiske kræftformer.
I starten af april har BioInvents partner ThromboGenics desuden fremlagt de første kliniske data fra et fase I/II studie med antistoffet THR-317, der er rettet mod PIGF-receptoren (Human Placental Growth Factor). THR-317 udvikles i forhold til behandling af øjensyndommen DME (Diabetic Macular Edema), som i ubehandlet tilstand kan føre til blindhed. THR-317 blev testet på 4 mg og 8 mg over 90 dage og behandlingen viste sig sikker. Desuden sås en dosisafhængig responsrate, hvilket i praksis udmålte sig ved at 30% af patienterne behandlet med 8 mg opnåede en forbedret synstest svarende til 15 bogstaver eller 3 linjer, mod bare 5,3% af patienterne behandlet med 4 mg THR-317. BioInvent er berettiget til royalties på 5% af alle indtægter som udviklingen af THR-317 genererer, mens ThromboGenics afholder alle udgifter. BioInvents aktiekurs er faldet med 2% og er nu i -7% siden begyndelsen af året.
Kanceras bestyrelse har foreslået gennemførelse af en emission med fortegningsret for eksisterende aktionærer med henblik på at rejse et provenu på ca. 60 mio. SEK. Emissionen garanteres op til 80% af selskabets nuværende aktionærer, men en endelig godkendelse er påkrævet på Kanceras ekstraordinære generalforsamling som afholdes d. 20. april. Formået med emissionen er at rejse kapital til gennemførelse af et fase IIa studie med det førende pipelineprojekt KAND567, som behandling mod hjerteskade fremkommet efter et hjerteanfald. Kancera har allerede fremlagt lovende fase I data med KAND567, der viser at doser op til 5-10 gange den forventede effektive dosis er sikre at anvende. Herudover ønsker selskabet at foretage afsluttende tox-studier med det prækliniske Tyrosine-protein kinase ROR1 udviklingsprojekt KAN0439834, med henblik på at rykke programmet tæt på den kliniske fase. For nyligt fremlagde selskabet prækliniske data der påviste, at KAN0439834 har en anti-tumor effekt i mus med CLL (Kronisk lymfatisk leukæmi). Kancera-aktien har reageret på emissionsplanerne med et fald på 38% og er nu i -36% for hele året.
Lundbeck meddeler, at man har opkøbt det schweiziske selskab Prexton Therapeutics med henblik på at få adgang til den kliniske udviklingskandidat foliglurax, som befinder sig i kliniske fase II studier til behandling af Parkinsons sygdom. I juli 2017 påbegyndtes fase II studiet som foretages i symptomatisk behandling til reduktion i OFF-time ved Parkinsons sygdom og dyskinesi, herunder Levodopa-induceret dyskinesi (LID). Der ventes resultater fra fase II studiet i løbet af 1.halvår 2019. Foliglurax virkningsmekanisme bestå i stimulering af et specifikt glutamatergt mål (mGluR4), der aktiverer et kompensatorisk neuronsystem i hjernen, som i det store hele er upåvirket af Parkinsons sygdom. Dyremodeller har påvist positive effekt i modeller af Parkinsons sygdom. Hensigten er at behandle motorsymptomer forbundet med Parkinsons sygdom, såsom rystebevægelser i hvile, muskelstivhed og ukontrollerede bevægelser (dyskinesi). Lundbeck betaler 100 mio. EUR for selskabet, og er herudover forpligtet til yderligere betalinger på op til 805 mio. EUR betinget af succesfuld klinisk og kommerciel udvikling af foliglurax. Lundbeck aktien ligger uforandret de seneste tre uger. Aktien er dermed fortsat i et plus på 8% siden nytår.
Novo Nordisk meddeler at once-weekly GLP1-analogen Ozempic er blevet godkendt i Japan, som en behandling mod diabetes type 2. Dermed er Ozempic nu godkendt i både USA, Europa og Japan. Lancering på det japanske marked forventes når tilskudsforhandlinger med de japanske myndigheder er afsluttede. Vedrørende basal-insulinen Tresiba har Novo Nordisk endvidere meddelt, at FDA har tilføjet positive effekter på hjerte/kar samt positive effekter i forhold til en reduktion i forekomsten af for lavt blodsukker (hypoglykæmi) til Tresiba-indlægssedlen. De positive effekter er observeret i dels det 7637 patienter store kardiovaskulære sikkerhedsstudie DEVOTE og dels i de to SWITCH studier, hvor man så positiv effekt i forhold til bivirkninger forårsaget af for lavt blodsukker. Novo Nordisks aktiekurs er faldet med 3% og er dermd i -13% for hele året.
Oncopeptides har afsluttet en rettet emission der har rejst et provenu på 314 mio. SEK før omkostninger. I alt er 3,98 mio. nye aktier til en tegningskurs på 79 SEK per aktie udstedt. Det samlede antal udestående aktier i selskabet stiger dermed med 10% til nu 43,8 mio. aktier udestående. Investorkredsen tæller blandt andet Industrifonden og lifescience-fonden HealthCap VI. Oncopeptides påtænker at anvende provenuet på at forberede en markedslancering af selskabets primære udviklingskandidat Ygalo (melfluten), som er en innovativ peptidase-potentiated alkylator (cellegift) målrettet behandlingen af blodkræft-sygdomme, herunder først og fremmest Multiple Myeloma (Myelomatose). Ygala befinder sig nu i afsluttende fase III studier i Multiple Myeloma med forventede data i sommeren 2019 og dermed potentiel markedslancering i 2020. Oncopeptides aktien er faldet med 11% og er nu -4% for hele 2018.



Intro-pris i 3 måneder
Få unik indsigt i de vigtigste erhvervsbegivenheder og dybdegående analyser, så du som investor, rådgiver og topleder kan handle proaktivt og kapitalisere på ændringer.
- Fuld adgang til ugebrev.dk
- Nyhedsmails med daglige opdateringer
- Ingen binding
199 kr./måned
Normalpris 349 kr./måned
199 kr./md. de første tre måneder,
herefter 349 kr./md.
Allerede abonnent? Log ind her











