Siden børsnoteringen ultimo juni sidste år har Calliditas Therapeutics igangsat deres fase-3 forsøg, mens aktien har mistet 2% svarende til en udvikling stort set på niveau med Nasdaq Biotechnology Index. Selskabets fremtid er meget afhængig af Nefecon, et lægemiddel som retter sig imod medicinsk behandling af den sjældne autoimmune kroniske nyresygdom IgA nefropati. Med de meget begrænsede muligheder for medicinsk behandling i dag, ser vi et betydeligt kurspotentiale i aktien på sigt.


IgA nefropati tilskrives en genetisk defekt og har sit udspring i den nederste del af tyndtarmen. Der er tale om en fejlkodning af antistoffet IgA, som mangler galaktoseenheden. Immunforsvaret reagerer på de fejlkodede antistoffer, som medfører ophobning af immunoglobulinkomplekser i nyrerne med efterfølgende betændelsestilstand og en gradvis nedsættelse af nyrefunktionen.
Calliditas’ lægemiddelkandidat Nefecon er en patenteret oral kapselformulering af kortikosteroidet budesonid, som medfører forbedret klinisk (controlled release) behandlingseffekt.
Fase-3 studie igangsat i november
Calliditas har gennemført markedets største placebokontrollerede kliniske IgA nefropati studie på 150 patienter, som tegner lovende. Patienterne i dette fase-2 studie havde proteinuri (forhøjet indhold af protein i urinen), og UPCR (urine protein creatinine ratio) blev benyttet som surrogatmarkør for behandlingseffekten.
De to behandlingsaktive arme fik henholdsvis 8 mg og 16 mg dosis dagligt. Behandlingseffekten var statistisk signifikant ved den høje dosis, hvor UPCR faldt med 29.3% (p=0.009). Behandlingseffekten varede ved i den efterfølgende 3 måneders opfølgningsperiode med et fald i UPCR på 32% i forhold til baseline, mens der hos placebopatienterne var tale om en svag stigning. EGFR-markøren (estimated glomerular filtration rate) for nyrefunktionen viste også en forbedring i den aktive gruppe i forhold til placebogruppen, svarende til en stabilisering af sygdomstilstanden.
Det igangværende fase-3 studie med opstart i november 2018 er et omfattende projekt helt i tråd med fase 2b studiets design. 450 patienter får en daglig dosis på 16mg over 9 måneder med proteinuri som primært klinisk endpoint. Resultatet af studiet på de første 200 patienter skal give adgang til accelereret godkendelse i USA og en betinget godkendelse i Europa hos EMA. Patienterne observeres herefter de efterfølgende 3 måneder med henblik på eftervisning af korrelationen imellem surrogatmarkøren proteinuri og eGFR. Herefter observeres patienterne over en længevarende periode.
Risikoen for at den uafhængige datakomité vil stoppe studiet før tid vurderes at være minimal pga. den veldokumenterede kliniske profil på Nefecon.
Konkurrentsituationen
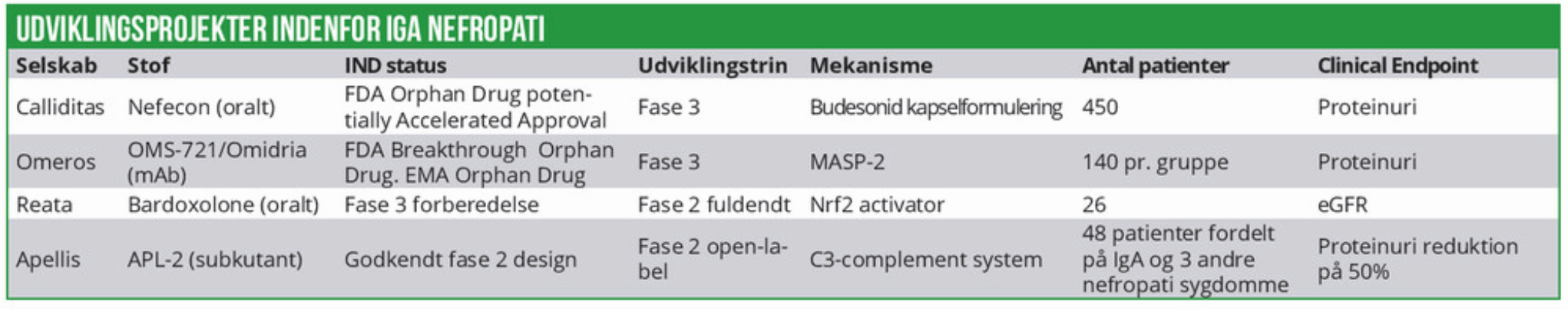
Calliditas har førertrøjen på indenfor IgA nefropati, men der er dog konkurrenter, som benytter stoffer med andre virkningsmekanismer. Blandt de primære konkurrenter kan nævnes Omeros, Reata og Apellis.
Amerikanske hedgefunds har udvist stor positiv interesse for Reata på det seneste. Reata forfølger udover IgA nefropati også fire andre sjældne kroniske nyresygdomme med to aktive stoffer bardoxolone og omaveloxolone. Resultatet af bardoxolone IgA nefropati fase-2 open label studiet var positivt. Ikke alene blev eGFR stabiliseret over tid, men efter 12 uger var der tale om en gennemsnitlig statistisk signifikant stigning på godt 17% i forhold til base line samtidig med, at UACR (urine albumin creatinine ratio) markøren blev stabiliseret. Reata forbereder nu et pivotalt/fase-3 studie.
Omeros’ OMS-721 (et monoklonalt antistof) viste i et mindre indledende open label fase-2 studie, hvor patienterne samtidig fik steroidbehandling, en forbedring i eGFR og UACR. Et efterfølgende placebokontrolleret 12 patient fase-2 studie faldt dog i umiddelbar betragtning uheldigt ud. Efter 18 ugers behandling var effekten målt på proteinuri den samme som i placeboarmen, nemlig -18%. I løbet af en uge faldt aktiekursen med 40%.
I forbindelse med Calliditas’ telefonkonference ovenpå på selskabets årsregnskab i sidste uge bagatelliserede Calliditas’ CEO Renee Aguiar-Lucander indirekte sandsynligheden for, at OMS-721 bliver en konkurrent med henvisning til ovennævnte studie. Ikke desto er det langt fra usandsynligt, at Omeros’ fase-3 studie alligevel vil lykkes. Det skyldes, at fase-2 studiet ikke var designet til at vise signifikans i forhold til placeboarmen, da patientprofilerne i de to arme var meget forskellige (især ift. alder og tid siden diagnose). Dels fordi patienterne ikke undergik samtidig steroidbehandling, som det var tilfældet i det indledende studie. I den efterfølgende 9 måneders opfølgningsperiode blev der således konstateret en nedsættelse af proteinuriniveauet på i gennemsnit markante 61%, hvilket indikerer en betydelig effekt på længere sigt af OMS-721, selvom der altså ikke var signifikant forskel i forhold til placeboarmen i selve studiet.
Apellis rekrutterer pt. til et fase 2 studie og APL-2’s potentiale er derfor usikkert. Udover de nævnte selskaber har Rigel og Merck KGaA fase-2 IgA nefropatiprojekter i udvikling.
I forhold til konkurrenterne har Calliditas fordel af Nefecons dokumenterede kliniske profil. Også det forhold, at Nefecon er oralt tæller positivt i modsætning til Apellis og Omeros’ lægemiddelkandidater. På langt sigt er det ikke usandsynligt, at lægemidler med forskellig virkningsmekanisme kan suppleres i kombinationsbehandling af IgA nefropati.
Dyr behandling sikrer kommercielt potentiale
Kronisk nyresygdom kræver ofte i den sene fase dialyse, som er meget omkostningstungt. I USA er omkostningerne til hæmodialyse på 42 mia. USD årligt (fordelt med anslået 70.000 til 200.000 USD pr. patient), og en nyretransplantation koster ca. 415.000 USD. Med behovet for bedre behandlingsmuligheder for kroniske nyrepatienter har FDA tydeligvis prioriteret nye lægemidler på området højt, og markedet vil sandsynligvis acceptere en relativ høj pris for forbedrede behandlingsmuligheder.
Calliditas har pt. ingen partner og vil i 2019 afsætte betydelige ressourcer til analysen af det amerikanske behandlingssystem indenfor kroniske nyresygdomme. Calliditas vil i markedsføringen af Nefecon fokusere på patienter med fremskreden sygdom (ERSD-patienter), som har et veldokumenteret behov for forbedret medicinsk behandling. ERSD-patienterne udgør ca. 40% af IgA nefropatipatienterne.
DCF-værdi på 79 SEK per aktie
I base case scenariet antager vi en Nefecon behandlingspris pr. år på 35.000 USD i USA. Pga. den relativt store kliniske dokumentation fra fase-2 studiet vurderes sandsynligheden for, at Nefecon når markedet til 65%. Det er lidt højere end industrigennemsnittet for Orphan Drugs indenfor autoimmune og inflammatoriske sygdomme. Det estimeres, at markedsandelen i ERSD-segmentet når 20%.
Calliditas planlægger at forfølge flere indikationer med Nefecon, herunder leverbetændelse (autoimmun hepatitis), som man lige har fået tildelt Orphan Drug status på. Nye indikationer vil på sigt kunne løfte Nefecon’s indtjeningspotentiale og forbedre selskabets risikoprofil, men på nuvæ-rende tidspunkt er de ikke tillagt nogen værdi i værdiansættelsen.
I base case scenariet er DCF-værdien 79 SEK per aktie og følsomheden overfor ændrede markedsandele fremgår af tabellen. En lidt mere alternativ multipel som ”Pris/Peak Sales” kan opgøres til 1,2. Det er lavt i forhold til gennemsnittet for amerikanske Nasdaq biotekselskaber, som normalt ligger omkring 2 til 3. Sammenligner man iøvrigt Calliditas’ markedsværdi med konkurrenterne synes den langt fra voldsom, som det fremgår af oversigten. Konkurrenterne har dog en bredere pipeline, og Omeros har et produkt på markedet allerede.
Kassebeholdningen på 646 mio. SEK forventes at række til finansieringen af IgA Nefropati fase-3 studiet, og dermed også forbi de altafgørende Nefecon IgA topline-data i 2. halvår 2020.
Nefecon har et betydeligt kommercielt indtjeningspotentiale i et patientsegment, hvor de medicinske behandlingsmuligheder pt. er utilfredsstillende. Calliditas har dog ikke erfaring med kommercialisering, hvilket ofte er en stor udfordring for biotekselskaber uden partnerskab. Calliditas har imidlertid i år ansat Andrew Udell med erfaring på området.
Med en fair værdi på 79 SEK har aktien et betydeligt kurspotentiale på sigt. På kort sigt hæmmes kurspotentialet af, at den primære kurstrigger (fase-3 data) først udløses i 2. halvår 2020, og i den mellemliggende periode kan kursudviklingen begrænses af markedets beskedne analysedækning af selskabet. Vi vælger derfor at sætte et mere afdæmpet 12 måneders kurstarget på 60 SEK.
Kurs på anbefalingsstidspunkt: 43,30 SEK
Kurstarget: 60 SEK (12 måneder)
Lars Hatholt
Calliditas indgår i Økonomisk Ugebrev Biotechs modelportefølje.



Intro-pris i 3 måneder
Få unik indsigt i de vigtigste erhvervsbegivenheder og dybdegående analyser, så du som investor, rådgiver og topleder kan handle proaktivt og kapitalisere på ændringer.
- Fuld adgang til ugebrev.dk
- Nyhedsmails med daglige opdateringer
- Ingen binding
199 kr./måned
Normalpris 349 kr./måned
199 kr./md. de første tre måneder,
herefter 349 kr./md.
Allerede abonnent? Log ind her











