Grafikken denne gang er uhyre interessant og tankevækkende ved første øjekast, men lad os slå det fast med det samme, at det umiddelbare billede dog næppe er den fulde sandhed. Der er en række faktorer, som kan ændre billedet og påvirke den dragende og umiddelbare konklusion om, at 2/3 af cancer-lægemidler bliver godkendt uden at have effekt på overlevelsen.
Andre faktorer er f.eks. Quality of Life, som slet ikke indgår i undersøgelsen, ligesom der også kan indtænkes mange usikkerheder omkring OS-fordele eller mangel på samme. Herunder tæller vi skiftende behandlingsregimer og meget konkret, at studier kan dække over store forskelle i forskellige patientgrupper, hvor nogle patienter slet ikke oplever effekt, mens en mindre gruppe oplever betydelig effekt uden, at en eventuelt samlet OS-effekt nødvendigvis er statistisk signifikant.
Hele 85 % af lægemidlerne er rettet mod metastatisk cancer og det åbner for meget komplekse behandlingsforløb og høj dødelighed.
“In conclusion, we found that less than one-third of drug indication approvals by the FDA have been shown to improve OS with a median 5 years on the US market. Of the drugs that are approved on a surrogate, only about half are tested for survival benefit, yet only about 20 % of the drugs not approved on a surrogate show OS benefit. Our results suggest persstent deficiencies in the US regulation of cancer drug products. Regulators are tolerating a high degree of uncertainty for these products.”
Vi er stødt på grafikken her, men den stammer oprindelige fra tidsskriftet Cancer Medicine, som er et fagfællebedømt tidsskrift, men ikke fra øverste hylde som eksempelvis The Lancet eller New England Journal of Medicine.
Originalartiklen har den noget kontroversielle Vinay Prasad fra FDA som medforfatter og kan læses i sine fulde form her. Vinay Prasad blev udnævnt som director for FDA’s CDER-afdeling af Robert Kennedy Jr. i foråret 2025, men trådte allerede tilbage i juli sidste år efter få måneder på posten efter intens kritik for sin indblanding i og håndtering af Sareptas lægemiddelansøgning for Elevidys. Han blev dog hurtigt hentet tilbage igen, men efter megen offentlig kritik af hans indblanding i Modernas ansøgning for deres influenza-vaccine tidligere i år, meldte han igen sin afgang. Denne kom ved udgangen af april i år. Derudover har der været forlydender om meget intern kritik i FDA af ledelsesstil m.m.
Efter dette hurtigere sidespring hopper vi tilbage til grafikken og artiklen, som er fra april 2024 og bærer titlen ”An empirical analysis of overall survival in drug approvals by the US FDA (2006–2023)”. Den undersøger 392 cancer-lægemidler, der er blevet godkendt i perioden 2006-2023 med sigte på at undersøge sammenhængen mellem godkendelse på baggrund af ”surrogat-endpoints” og Overall Survival (OS). Sidstnævnte er i manges øjne ”Gold Standard”, og også for patienterne det reelle primære endpoint og vigtigste mål for effekt.
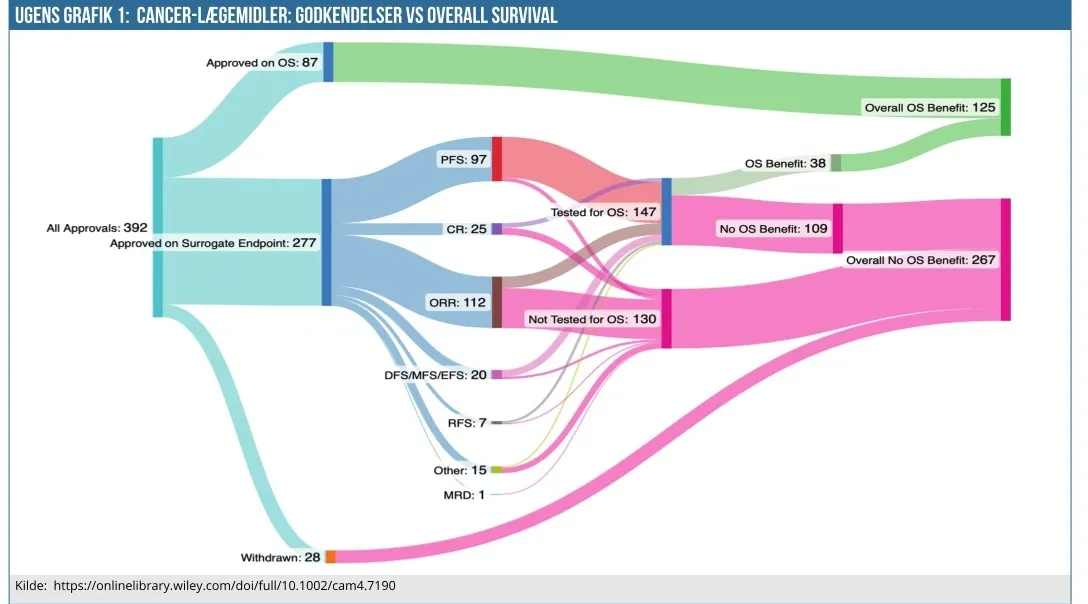
I venstre side af grafikken har vi de 392 cancer-lægemidler, der indgår i datasættet. Ude til højre har vi de to hovedkonklusionsgrupper, en med de 125 lægemidler der har påvist en OS-effekt, og de 267 lægemidler, der ikke har påvist en OS-effekt. Altså er det i grove træk kun hver 3. lægemiddel, der i et studie har vist en egentlig effekt på overlevelsen.
Alt mellem venstre og højre side af grafikken søger at vise, hvordan lægemidler når fra godkendelse og hen til enten den ene eller anden hovedkonklusionsgruppe. F.eks. ser vi, at 87 lægemidler tager den øverste ”vej”, da de blev direkte godkendt med en positiv OS-effekt. Tilsvarende har vi nederst den gruppe af 28 lægemidler, der efter godkendelse helt har fået trukket sin godkendelse tilbage.
I midtergruppen på 277 lægemidler finder vi den interessante gruppe, der er blevet godkendt på baggrund af surrogat-endemål. Disse surrogat-endemål er første ”stop” i midtergruppens vej mod højre side, og de fordeler sig med ORR (112) og PFS (97) som de væsentligste endpoints, mens de øvrige (og mindre) grupper er CR (complete response) med 26 og event-free/disease-free/metastasis-free survival med 20 og relapse-free survival med 7.
Næste stop er, om der efterfølgende er gennemførte OS-studier, hvilket er tilfældet for 147 lægemidler, mens 130 lægemidler ikke har OS-studier. Sidstnævnte tager den direkte vej ud til højre og udgør en del af de 267, der ikke har en påvist OS-effekt. De 147 lægemidler, der har efterfølgende OS-studier, fortsætter deres vej ud til højre afhængig af, om studiet viste en OS-effekt eller ej.
Spørgsmålet, man som læser grundlæggende sidder tilbage med, er, om de valgte surrogat-endpoints i sidste ende er valide retningspile for effekten af et cancer-lægemiddel?
Grafikken og artiklen leder dermed direkte videre til det mere overordnede dilemma om at få lægemidler hurtigere godkendt og frem til patienterne, samtidig med at man skal sikre, at lægemidlerne er effektive med færrest mulige bivirkninger.
Undersøgelse af ”Accelerated approval”
Det leder os videre til dagens anden grafik, som er noget enklere og udelukkende fokuserer på de cancer-lægemidler, der er godkendt via den regulatoriske vej accelerated approval i perioden 2013 til 2023. I nr. 6/2026 viste vi en grafik over de forskellige genveje til en hurtigere sagsbehandling og godkendelse hos FDA.
Grafikken stammer oprindeligt fra en artikel i det videnskabelige tidsskrift JAMA (Journal of the American Medical Association) og undersøger den kliniske fordel af cancer-lægemidler med accelerated approval og på hvilket grundlag, de efterfølgende konverteres til fuld godkendelse.
”What is the clinical benefit of cancer drugs granted accelerated approval, and on what basis are they converted to regular approval?” er artiklens hovedspørgsmål.
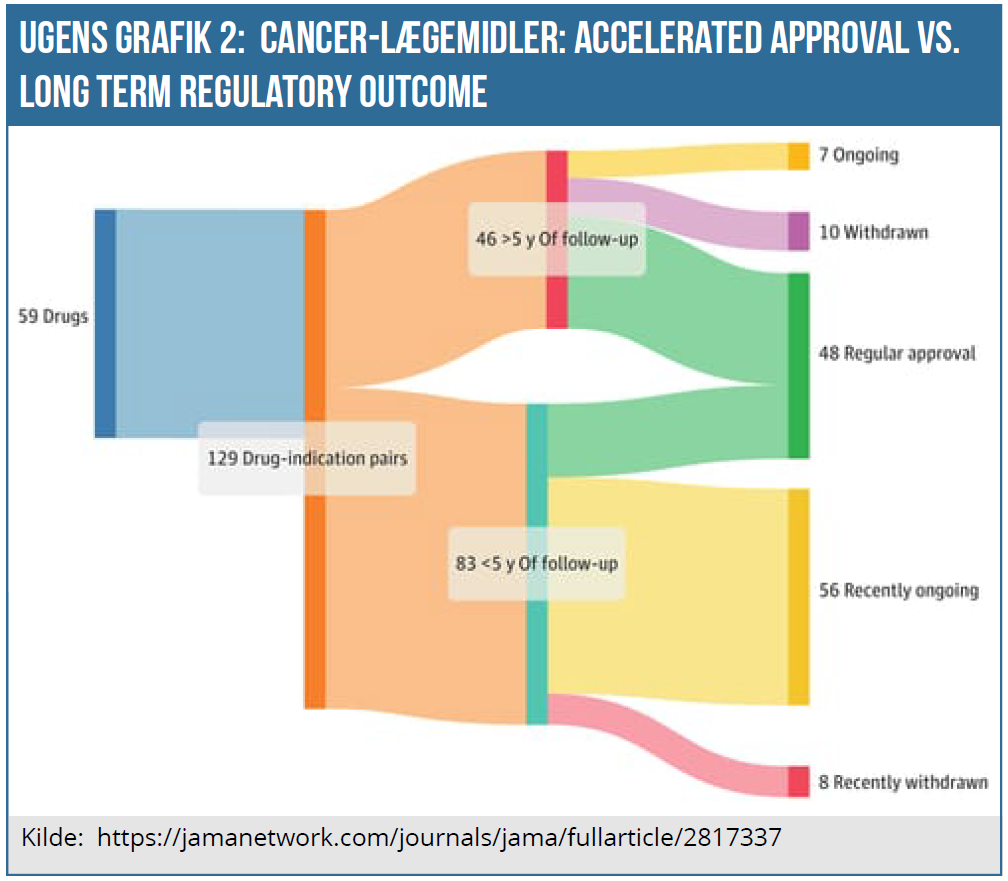
Artiklen har fundet 129 cancerlægemidler (”drug indication pairs”) med accelerated approval i perioden, fordelt på 59 forskellige lægemidler. Altså er i gennemsnit tale om, at hvert lægemiddel har fået accelerated approval i 2 forskellige indikationer.
Antallet på 129 kan synes højt, men det hænger også sammen med, at 80 % af alle accelerated approvals er givet til cancer-lægemidler.
De 129 lægemiddel-indikationer (en fuld liste findes i artiklens bilag 1) er delt op i to grupper, afhængig af om der er mulighed for mindst 5 års opfølgning eller ej. Derefter er der tjekket for, om der er tildelt fuld godkendelse, eller om godkendelsen er trukket tilbage, eller om der endnu ikke er data.
Artiklen undersøger herudover også en række andre faktorer, såsom tidslinjer til fuld godkendelse og på hvilket grundlag, man efterfølgende opnåede godkendelse.
Status er, at 48 ud af 129 har fået en efterfølgende fuld godkendelse. 18 (10+8) har fået trukket godkendelsen tilbage, mens 63 (56+7) stadig afventer en klinisk afklaring. Af de 48 med fuld godkendelse havde 19 (40 %) efterfølgende vist en positiv OS-effekt, mens 41 % (19 ud af 46) ikke viste en bedring i OS eller Quality of Life efter mere end 5 års opfølgning. Og med en konklusion som denne “Most cancer drugs granted accelerated approval did not demonstrate benefit in overall survival or quality of life within 5 years of accelerated approval. Patients should be clearly informed about the cancer drugs that use the accelerated approval pathway and do not end up showing benefits in patient-centered clinical outcomes.” slutter ringen og bringer os tilbage til den første grafik.
Lægemiddeludvikling og godkendelse er i sandhed en kompleks størrelse, og det er en konklusion som alle bør kunne være enige om, uanset om er Vinay Prasad eller hans modsætning.
Kilde 1: https://onlinelibrary.wiley.com/doi/full/10.1002/cam4.7190 via @cremieuxrecueil
Kilde 2: https://jamanetwork.com/journals/jama/fullarticle/2817337 via @cremieuxrecueil
Steen Albrechtsen